ルイジ・リカルディ 1 、 ローザ・マゼオ 2,*©、 アンジェロ・ラーffアエレ・マルコトリジャーノ 1 , グリエルモ・ライナルディ 3 、パオロ・イオビエノ 4 、ヴィト・ゾンノ 1 、ステファノ・パヴァン 1年© コンチェッタ・ロッティ 2,*
- 1 土壌、植物および食品科学科、植物遺伝学および育種ユニット バーリ大学、アメンドラ 165/A 経由、70125 バーリ、イタリア。 luigi.ricciardi@uniba.it (LR);angelo.marcotrigiano@uniba.it (腕); vito.zonno@uniba.it (VZ); stefano.pavan@uniba.it (SP)
- 2 農業、食品、環境科学科、フォッジャ大学、Via Napoli 25、71122 フォッジャ、イタリア
- 3 バイオサイエンス、バイオテクノロジー、バイオ医薬品学科、バーリ大学、Via Orabona 4、70125 バーリ、イタリア。 guglielmo.rainaldi@uniba.it
- 4 Department of Energy Technologies, Bioenergy, Biorefinery and Green Chemistry Division, ENEA Trisaia Research Center, SS 106 Ionica, km 419+500, 75026 Rotondella (MT), Italy; paolo.iovieno@enea.it
* 対応: rosa.mazzeo@unifg.it (RM); concetta.lotti@unifg.it (CL)
要約:
タマネギ (ネギ L.) は、世界で 11 番目に重要な野菜作物であり、その健康上の利点が広く評価されています。 その重要な経済的重要性と機能性食品としてのその価値にもかかわらず、タマネギはその遺伝的多様性に関して十分に調査されていません. ここでは、バーリ県 (イタリア南部のプーリア州) の小さな町で 13 年前から栽培されてきた在来種である「アクアヴィーバ赤タマネギ」(ARO) の遺伝的変異を調査しました。 XNUMX のマイクロ サテライト マーカーのセットを使用して、XNUMX の ARO 集団と XNUMX つの一般的な商用タイプからなる生殖質コレクションの遺伝的変異を調査しました。 パラメトリック法およびノンパラメトリック法による遺伝子構造の分析により、ARO が明確に定義された遺伝子プールを表していることが強調されました。これは、よく誤解されるトロペアおよびモントロの在来種とは明らかに異なります。 通常は新鮮な消費に使用される球根の説明を提供するために、可溶性固形分と辛味が評価され、上記のXNUMXつの在来種に関してAROでより高い甘さが示されました. 全体として、本研究は、商業詐欺を制限し、小規模農家の収入を改善するのに貢献できる品質ラベルを通じて促進される可能性のあるAROの将来の価値化に役立ちます。
概要
アリウム属には約 750 の種が含まれており [1]、その中でタマネギ (Allium cepa L.、2n = 2x =16) は最も普及している種の 97.9 つです。 A. cepa は隔年サイクルと異系交配の生殖行動を持っています。 今日、タマネギの世界生産量 (2 Mt) は、トマトに次いで 1550 番目に重要な野菜作物になっています [3]。 タマネギの球根は、古くから食用や民間薬として利用されてきました。 実際、古代エジプト人は、紀元前 XNUMX 年の医療パピルスである Codex Ebers [XNUMX] で、ニンニクとタマネギの使用に基づいたいくつかの治療法をすでに報告しています。
この多目的で健康的な野菜は、生、生、または加工品として消費され、多くの料理の味を引き立てるために使用されます. 最近のいくつかの研究では、タマネギの摂取が心血管疾患 [4,5]、肥満 [6]、糖尿病 [7]、およびさまざまな形態の癌 [8–10] のリスクを低下させる可能性があると主張しています。 タマネギの健康上の妥当性は、多くの場合、フラボノイドとアルキルシステインスルホキシド (ACSO) という XNUMX つのクラスの栄養補助化合物が高レベルで含まれていることに起因します。 最初のクラスには、フラボノールとアントシアニンが含まれます。 ケルセチンは主要な検出可能なフラボノールであり、フリーラジカル消去と遷移金属イオン結合における強力な抗酸化および抗炎症特性で知られています 【11]; 一方、アントシアニンは、いくつかのタマネギの品種に赤/紫の色を与えます. ACSOに関しては、最も豊富なのはイソアリイン[(+)-トランス-S-1-プロペニル-L-システインスルホキシド]です。 【12]タマネギの刺激的な香りと味の間接的な原因である、細胞に保存されている非揮発性および非タンパク質原性硫黄アミノ酸 【13]. 組織が破壊されると、イソアリインはアリイナーゼという酵素によって切断され、一連の揮発性化合物 (ピルビン酸、アンモニア、チオスルホン酸、プロパンチオール S-オキシド) を生成します。 【14]. タマネギの辛味は、多くの場合、加水分解によって生成されるピルビン酸の生重量 XNUMX グラムあたりの量として測定されます。 [15、16].
地中海沿岸の国々では、二次多様性センターのXNUMXつとして提案されています A.cepa [17、18]、タマネギの球根は、形状、サイズ、色、乾物、辛味において幅広いバリエーションを示します [19~22】. さらに、硫黄ベースの施肥、農業慣行、土壌の種類、気候条件、および栽培品種または在来種の遺伝子型は、独特の官能的および栄養価を付与することにより、球根の品質に影響を与える可能性があります [23~27】. イタリアでは、タマネギの生殖質が広く入手できるにもかかわらず、科学的研究の対象となり、適切に特徴付けられているタマネギの品種はごくわずかです。 [28、29].
植物遺伝資源の適切な保護を保証し、バリューチェーンにおける特定の遺伝子型の使用を促進するためには、農業生物多様性の徹底的な遺伝的および表現型の特徴付けが不可欠です [30~32】. シンプル シーケンス リピート (SSR) マーカーは、マッピングによく選択されています。 [33~35】、DNAフィンガープリンティングと品種識別 [36~38】、および在来種内および在来種間の遺伝的変異性の信頼できる推定 [39~42】遺伝子座特異的、複数対立遺伝子、共優性遺伝、再現性が高く、自動ジェノタイピングに適しているためです。
本研究では、バーリ県のアクアヴィヴァ デッレ フォンティの町の小さな地域で有機農法に従って栽培されているプーリアの伝統的な在来種である「アクアヴィヴァ レッド オニオン」(ARO)に注目しました。 (南イタリア、プーリア州)。 この在来種の球根は大きく、平らで赤い色をしており、主に地元のレシピで使用されています. ARO は「スローフードプレシジウム」の品質マークを取得しましたが、その生産はさらに促進され、保護された地理的表示 (PGI) や保護された原産地呼称 (POD) などの欧州連合の品質マークによって保護される可能性があります。商業詐欺を防止し、小規模農家の収入を改善します。 ここで、SSR分子マーカーは、ARO集団間の遺伝的変異を評価し、この在来種を他のXNUMXつの南イタリアの赤タマネギの在来種と区別するための強力なツールとして使用されました。 さらに、市場の需要との関連でAROフレーバーを評価するために、辛味と可溶性固形分を推定しました。
結果
Acquaviva赤タマネギ生殖質コレクションの確立と形態学的特徴付け
BiodiverSO プーリア地域プロジェクトの枠組みで農家から寄贈された ARO 在来種の 13 個体群の種子を使用して、ARO 生殖質コレクションを確立しました。
球根、皮、および果肉に関連する形態学的記述子は、ARO 生殖質と XNUMX つのタマネギの在来種で収集されました. 1). すべての ARO 球根は平らで、さまざまな色合いの赤い外皮と果肉が特徴でした。 対照的に、TRO球根の肉は完全に赤く、MCO球根の肉は色素沈着が不十分でした(表S1)。 生化学的分析により、固形の可溶分と辛味を評価することができました。 表に報告されているように 1, ARO 個体群の球根の固形溶解量の平均値は 7.60 で、6.00 (ARO12) から 9.50° Brix (ARO11 および ARO13) の範囲でした。 この値は、TRO および MCO 在来種の推定値 (それぞれ 4.25 および 6.00° Brix) よりも高かった。

表1。 「Acquaviva Red Onion」(ARO)、「Tropea Red Onion」(TRO)、および「Montoro Copper Onion」(MCO)の集団で評価された固形溶解性含有量と辛味値 *.
| CODE | 可溶性固形分(Brix) | 辛味(pモルグ–1FW) | ||
| 平均 | CV y (%) | 平均 | CV y (%) | |
| ARO1 | 6.25D * | 5.65 | 腹筋5.84 * | 23.78 |
| ARO2 | 7.25 DC | 4.87 | 6.51 | 22.98 |
| ARO3 | 7.50 BCD | 9.42 | 5.28アブ | 22.88 |
| ARO4 | 7.50 BCD | 0.00 | 6.97 | 3.74 |
| ARO 5 | 7.50 BCD | 0.00 | 6.80 | 9.68 |
| ARO6 | 6.25 D | 5.65 | 4.51アブ | 39.18 |
| ARO7 | 7.25 DC | 4.87 | 5.25アブ | 15.44 |
| ARO8 | 9.00 AB | 0.00 | 7.04 | 3.49 |
| ARO9 | 8.25 ABC | 4.28 | 6.84 | 0.15 |
| ARO10 | 7.00 DC | 0.00 | 5.94アブ | 6.57 |
| ARO11 | 9.50 A | 7.44 | 5.54アブ | 16.43 |
| ARO12 | 6.00 D | 0.00 | 4.91アブ | 9.70 |
| ARO13 | 9.50 A | 7.44 | 6.63 | 24.93 |
| MCO | 6.00 D | 0.00 | 4.18アブ | 2.66 |
| トロ1 | 4.25 E | 8.31 | 2.80 B | 2.10 |
| トロ2 | 4.25 E | 8.31 | 4.28アブ | 4.79 |
* 大文字または小文字の同じ文字の意味は、それぞれ 0.01P または 0.05P で統計的に差がありません (SNK のテスト)。 y 変動係数。
ピルビン酸含有量によって評価された ARO 辛味の平均値は 6.00 で、4.51 pmol g の範囲でした。-1 FW (ARO6) から 7.04 (ARO8)。 この値は、TRO および MCO 在来種で推定された値よりも高かった (3.54 pmol g-1 FW と 4.18 pmol g-1 それぞれFW)。
SSR多型とアクセッション間の遺伝的関係
本研究では、11 のテストされた SSR プライマーの組み合わせのうち 37 が単一遺伝子座多型を提供しました。 全体として、55 人の個人で 320 の対立遺伝子が検出され、遺伝子座あたりの対立遺伝子数は 2 (ACM147 および ACM 504) から 11 (ACM132) の範囲で、平均値は 5 対立遺伝子でした (表 2). 個々の集団では、対立遺伝子の数 (Na) は 1.94 (ACM147 および ACM504) から 5.38 (ACM132) の範囲でしたが、対立遺伝子の有効数 (Ne) は 1.41 (ACM152) から 2.82 (ACM449) の範囲でした。 不一致 Na 値と Ne 値の間の差は、集団内に頻度の低い対立遺伝子が存在し、少数の対立遺伝子が優勢であるためです。 観測されたヘテロ接合性 (Ho) の最高値は、ACM138 および ACM449 (0.62) で強調表示されましたが、最低値は ACM152 (0.25) に関連していました。 パニック集団における理論上の予想に対応する予想ヘテロ接合性 (He) は、0.37 (ACM504) から 0.61 (ACM132、ACM138、および ACM449) の範囲でした。 ライト固視指数 (Fis) は、すべてのマーカーでゼロに近い値 (平均 0.05) を示し、異系交配種で予想されるように、観察されたヘテロ接合性レベルと予想されるヘテロ接合性レベルの間で類似した値を示しています。 遺伝子フィンガープリンティングにおける個々の SSR マーカーの効率は、多型情報コンテンツ (PIC) インデックスによって推定され、平均値は 0.48 で、範囲は 0.33 (ACM504) から 0.67 (ACM132) でした。 別の効率指数であるシャノンの情報指数 (I) は平均値 0.84 を示し、推定値は 0.45 (ACM152) から 1.20 (ACM132) の範囲でした。
表2。 ARO、TRO、および MCO 集団の遺伝的多様性を推定するために使用される 11 の SSR マーカーの多型の特徴。 対立遺伝子の総数 (Na)、バンド サイズの範囲、および多型情報コンテンツ (PIC) インデックス この研究で遺伝子型が特定された 320 人の個体の総数を参照してください。 対立遺伝子の数 (Na)、有効な対立遺伝子の数 (Ne)、観測されたヘテロ接合性 (Ho)、予想されるヘテロ接合性 (He)、固着指数 (Fis)、およびシャノンの情報指数 (I) は、16 の母集団から計算された平均値を指し、それぞれが 20 人の個人によって構成されています。
| 軌跡。 | 合計Na | サイズ範囲 (bp) | PIC | 平均 | |||||
| Na | Ne | Ho | He | I | Fis | ||||
| ACM91 | 4 | 189-205 | 0.40 | 2.63 | 1.72 | 0.38 | 0.39 | 0.66 | 0.04 |
| ACM101 | 4 | 229-241 | 0.52 | 2.94 | 2.37 | 0.53 | 0.56 | 0.92 | 0.06 |
| ACM132 | 11 | 186-248 | 0.67 | 5.38 | 2.78 | 0.55 | 0.61 | 1.20 | 0.09 |
| ACM138 | 5 | 242-272 | 0.66 | 3.69 | 2.82 | 0.62 | 0.61 | 1.09 | -0.02 |
| ACM147 | 2 | 264-266 | 0.37 | 1.94 | 1.83 | 0.44 | 0.44 | 0.62 | -0.01 |
| ACM152 | 4 | 228-244 | 0.25 | 2.38 | 1.41 | 0.25 | 0.27 | 0.45 | 0.07 |
| ACM235 | 4 | 286-298 | 0.41 | 2.81 | 1.77 | 0.44 | 0.41 | 0.72 | -0.06 |
| ACM446 | 6 | 108-120 | 0.56 | 3.50 | 2.48 | 0.49 | 0.58 | 1.01 | 0.16 |
| ACM449 | 8 | 120-140 | 0.66 | 4.88 | 2.82 | 0.62 | 0.61 | 1.18 | -0.03 |
| ACM463 | 5 | 202-210 | 0.47 | 3.38 | 1.95 | 0.46 | 0.48 | 0.83 | 0.05 |
| ACM504 | 2 | 188-192 | 0.33 | 1.94 | 1.64 | 0.30 | 0.37 | 0.54 | 0.20 |
| 平均 | 5 | 0.48 | 3.22 | 2.15 | 0.46 | 0.48 | 0.84 | 0.05 |
集団の中で、ARO3、ARO6、ARO8、ARO10、TRO1、および MCO は高レベルの遺伝的変異 (Ho > 0.5) を示しましたが、集団 ARO7 (Ho = 0.27) では最も低い多様性が観察されました (補足表 S2)。 全体として、表示されたすべての加盟国 Fis ゼロに近い値 (Fis 平均値 = 0.054)、ランダム交配条件下で予想されるように。
分子分散と遺伝子構造の解析
集団間および集団内の遺伝的変異の階層的分割は、AMOVA によって計算されました。 結果は、集団内の遺伝的変異のかなりの部分 (87%) を浮き彫りにしました。 人口間の変動は 13% で、非常に有意でした (P < 0.001) (表 3). 0.002 (ARO2/ARO10) から 0.468 (ARO7/TRO2) の範囲のライトの Fst 凝視指数に類似した Fpt パラメータのペアワイズ値は有意でした (P < 0.05)、3 回のペアワイズ比較を除く (補足表 SXNUMX)。
表3。 320の集団からの16の遺伝子型の分子分散の分析 アリウムセパ L.
| ソース | df | 平方和 | 分散推定 | 分散(%) | Fpt | P |
| 人口間で | 15 | 458.63 | 1.16 | 視聴者の38%が | ||
| 集団内 | 304 | 2272.99 | 7.50 | 視聴者の38%が | 0.134 | 0.001 |
| トータル | 319 | 2731.62 | 8.66 |
における遺伝子構造の調査 A.cepa この研究で遺伝子型を特定したコレクションは、ソフトウェアSTRUCTUREに実装された混合モデルベースのクラスタリング分析によって実行されました。 Evanno AK メソッドは、2 つのクラスター (K = XNUMX) への細分化を提案しました。 データセット,番目とe 次の 最高のPEKでak = 5 (supplementaiv Rgure) S1)。 A フォーク = 2、 a馬力op計算wお尻igned それもnOf XNUMXつのクラスター rnernbertoip 係数 (q) > 0.7。 としてho勝つ フィギュア 2a、最初のクラスター (S1 という名前) には MCO とすべての ARO 集団が含まれていましたが、S2 クラスターには 5 つの TRO 集団がグループ化されていました。 K = XNUMX で、データセットのより深い説明を提供します (図 2b)、登録の 75% が 1 つのクラスターの 2 つに割り当てられました。 ARO (S0.7) と TRO (S3) の分離が確認されましたが、一部の ARO 集団は混合 (q < 4) または 7 つの新しいクラスター S12 と S5 (それぞれ AROXNUMX と AROXNUMX) で別々にグループ化されていました。 興味深いことに、MCO コマーシャル タイプは、プーリア赤タマネギから分離された明確なクラスター (SXNUMX) を形成しました。
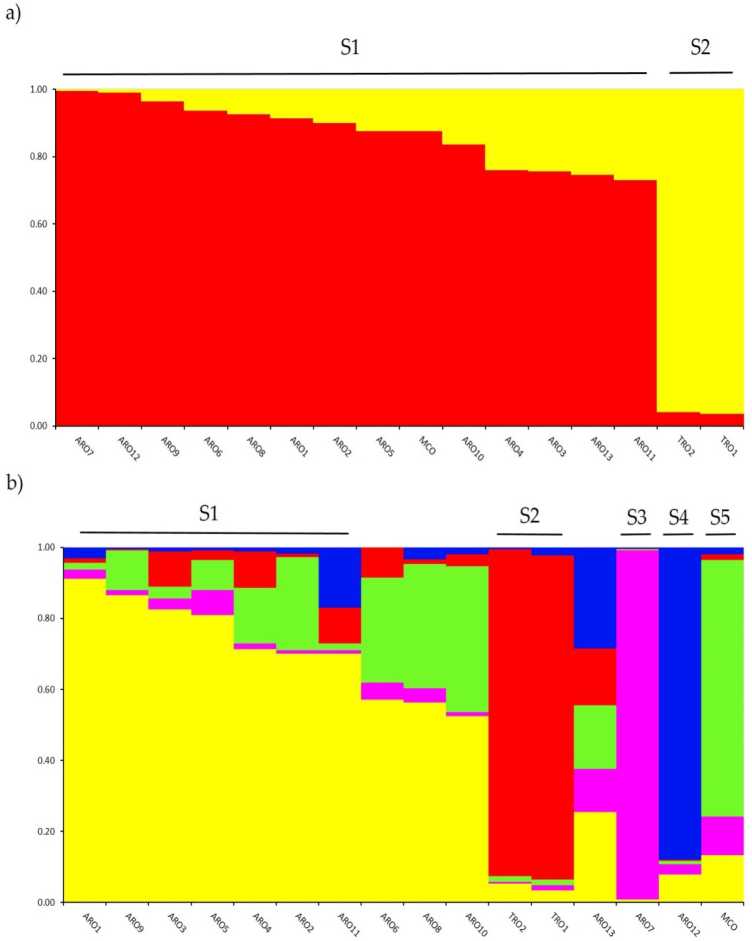
集団間の遺伝的関係
遺伝的多様性の樹状図を描くことを許可されたSSR多型と系統解析の結果を図に示します 3a. ここでは、生殖質コレクションは、ブートストラップ値によって強くサポートされている 7 つのグループに分割されました。 ARO12 と AROXNUMX の集団は、残りの集団からすぐに分離され、XNUMX つの異なるクラスターが形成されました。 XNUMX 番目のクラスターには、TRO の XNUMX つの商用集団が含まれていました。一方、XNUMX 番目のノードは、MCO を XNUMX の ARO 集団から分割しました。 集団間で発生する遺伝的関係は、主座標分析(PCoA)によってさらに調査されました(図 3b)。 前に強調したように、ARO 集団は、PCoA プロットの孤立した位置に現れた ARO12 と ARO7 を除いて、しっかりとグループ化されていました。 XNUMX つの TRO と MCO 集団は、プロットの右下のパネルに散らばっていました。
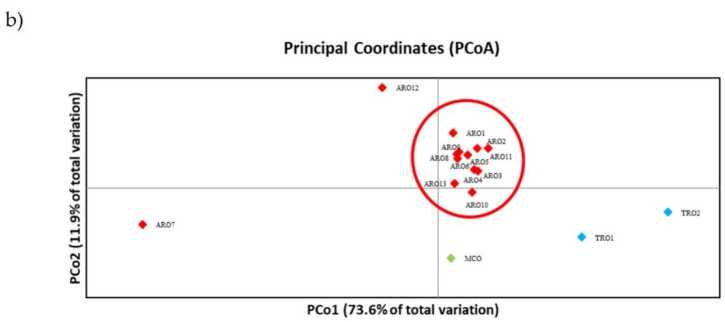
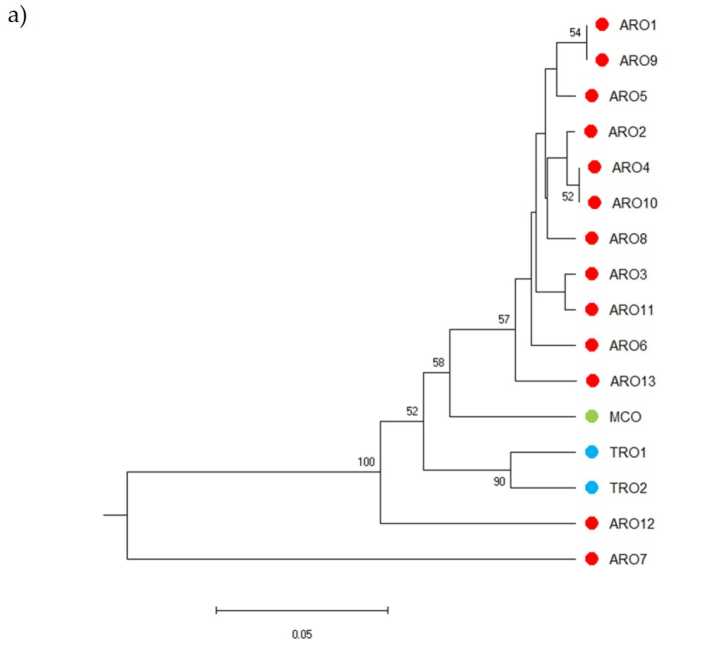
図3。 16の遺伝的多様性 A.cepa SSRプロファイルに基づいて、この研究で特徴付けられた集団。 (a) 遺伝的距離の UPGMA デンドログラム。 50 を超えるブートストラップ サポート値は、対応するノードの上に示されます。 (b) 主成分分析 (PCoA)。 赤丸で囲まれたクラスターは、系統解析によって生成されたグループと完全に一致し、11のAROアクセッションで構成されています。
議論
南イタリアで伝統的に栽培されている大量の農業生物多様性の中で、タマネギの在来種は、遺伝的浸食のリスクと現代の栽培品種による代替の脅威から保護する必要があるニッチな製品を表しています. 地元の遺産と強く結びついたプーリア地域の遺伝資源の収集、特徴付け、促進、保護を目的とした地域プロジェクト BiodiverSO の枠組みの中で、ARO 在来種の 13 個体群の種子コレクションを確立しました。 DNA 多型と XNUMX つの生化学的パラメーター、フレーバー特性に関連し、新鮮な未調理製品の受け入れにとって重要な可溶性固形物とピルビン酸含有量の観点から、ARO 変動の最初の評価を報告しました。 さらに、ARO 在来種のデータを、よく間違えられる他の XNUMX つの有色タマネギ在来種で収集されたデータと比較しました。
サツマイモ業界のガイドラインによると、生化学的分析により、高い可溶性固形分と中程度の辛味に関連する 13 の ARO 集団の甘さが強調されました。 【31]. ARO の球根は、TRO および MCO 在来種の球根よりも甘く、わずかに高い辛味を示しました。 ただし、タマネギの甘さは糖度と辛味のバランスによるものであるため、この特徴付けは、通常は農家が形態のみに基づいて行う、価値のある遺伝子型の選択をサポートするのに役立ちます。
SSR マーカーは、Acquaviva delle Fonti の町などの狭い生育地域内で収集されたにもかかわらず、遺伝子型を識別するための有用なツールであることが確認されました。 選択されたマーカーは、以前に報告されたマーカーよりも多くの対立遺伝子を示しました。 【43] および 【44]、しかしによって報告されたマーカーよりも低い 【45]. さらに、マーカーのセットの 50% が 0.5 を超える PIC インデックス値を示し、コレクション内の集団を識別するのに適していることが証明されました。 【46]. 集団内の多様性の評価により、Ho と He の間で同様の値が明らかになったため、Fi が低くなりましたs 値。 これは、アウトクロスの性質と一致しています。 A.セパ、 近親交配のうつ病に深刻に苦しんでいる 【47]. 全体的なFis この研究で考慮されたタマネギ集団で計算された値(0.054)は、以前に報告された値よりも低かった 【45] (0.22)であり、によって見つかったものとほぼ同じです 【31] (0.08)と 【48] (0.00) スペイン北西部とニジェールのタマネギ在来種の遺伝的多様性をそれぞれ評価した。 ARO 個体群における注目すべきレベルのヘテロ接合性は、プーリアが多くの園芸種の多様性の中心であるという考えを補強します。 [32、42、49~51】.
AMOVA は、この研究で遺伝子型が特定されたコレクションのほとんどの分子変異が集団内にあることを強調しました。 しかし、集団間の有意な遺伝的差異 (FPT 値) は、遺伝的層別化の発生を明らかにしました。 実際、私たちの結果は、ほとんどの ARO 集団に遺伝的均一性が存在し、明確に定義されたクラスターを形成していることを示していましたが、ARO7 および ARO12 集団は明確に異なる遺伝的プロファイルを示しました。 この結果は、集団が収集された XNUMX つの農家が使用した種子の起源が異なるためである可能性があります。 さらに、得られた結果に基づいて、ARO在来種は遺伝子レベルでTROおよびMCO在来種とは明らかに異なると考えることができます。 最近の研究では、 【29] 「Acquaviva」、「Tropea」、「Montoro」など、いくつかのイタリアのタマネギ在来種の遺伝的多様性を評価しました。 著者らはより広いタマネギ コレクションの遺伝的多様性を評価するために SNP マーカーを使用しましたが、ジェノタイピングでは「トロペア」および「モントロ」タマネギから「アクアビバ」を識別することができませんでした。 おそらく、この不一致は、発見された低い平均 PIC 値 (0.292) によるものであり、 【29]. さらに、彼らのイタリア人クラスターにおける部分構造の存在を調査するために、コレクションの残りの部分とは別にイタリア人の遺伝子型を分析する方がよいでしょう。 おそらく、経験的選択の下での地理的層別化または形質に関連する遺伝的多様性のパターンを視覚化することができたでしょう。
結論として、本研究は、地元の文化遺産に関連し、農家にとって経済的に重要なタマネギ在来種に関する包括的な報告を表しています。 私たちの結果は、いくつかの例外を除いて、ARO は明確に定義された遺伝子プールによって特徴付けられ、遺伝的侵食のリスクから保護するに値することを強調しています。 したがって、遺伝的多様性のこの貴重なソースの代表的なコレクションの確立は非常に重要です。 最後に、ARO の遺伝的および表現型の特徴付けは、欧州連合から品質マークを取得するのに役立つ可能性があります。
材料と方法
生殖質収集、植物材料、および DNA 抽出
ARO 在来種の 13 個体群のセットが、プーリア地域プロジェクト (BiodiverSO: https://www.biodiversitapuglia.it/)、イタリアのバーリ県にあるアプリアの小さな町「アクアヴィーバ デッレ フォンティ」で実施された一連のミッションを通じて。 各登録の収集サイトは、地理情報システム(GIS)を介してマッピングされ、表に報告されています 4. さらに、TRO在来種からの41つの集団とMCO在来種からの1つの集団が本研究に含まれ、参照として使用されました。 すべての植物材料は、バーリ大学の実験農場「P Martucci」(北緯 22.08 度 16 分 54 秒 25.95 秒、東経 XNUMX 度 XNUMX 分 XNUMX 秒 XNUMX 秒)の同じ環境条件で、他の動物との交配を避けるために保護ケージの下で栽培されました。クロバエによる個体群内受粉の保証 (ルシリアシーザー)。 16の集団は、球根のサイズと形状、および肌と肉の色に関連する形質について特徴付けられました(表S1)。 さらに、ハンドヘルド屈折計を使用して固形可溶分アッセイを実施し、2,4-ジニトロフェニルヒドラジン(0.125%)を添加したタマネギジュースサンプルの辛味を測定しました。 v/v で報告されているように、2 nm での吸光度を評価します。 【31]. ダンカンの多重範囲検定と SNK 検定を実行して、有意差の存在を判断しました。
表4。 この研究で収集され、遺伝子型が特定された集団のリスト。 各集団、識別コード、ローカル名、GPS 座標、および種子を保存する遺伝子バンクについて報告されます。
| Code | 名前 | GPS座標 | ジーンバンク y |
| ARO1 | チポラ ロッサ ディ アクアヴィーヴァ | 40°54’21.708″ N 16°49’1.631” E | Di.SSPA |
| ARO2 | チポラ ロッサ ディ アクアヴィーヴァ | 40°53’14.28″ N 16°48’56.879” E | Di.SSPA |
| ARO3 | チポラ ロッサ ディ アクアヴィーヴァ | 40°54’11.304″ N 16°49’13.079” E | Di.SSPA |
| ARO4 | チポラ ロッサ ディ アクアヴィーヴァ | 40°54’3.348″ N 16°40’27.011” E | Di.SSPA |
| ARO5 | チポラ ロッサ ディ アクアヴィーヴァ | 40°51’59.76″ N 16°53’0.527” E | Di.SSPA |
| ARO6 | チポラ ロッサ ディ アクアヴィーヴァ | 40°52’48.72″ N 16°49’43.247” E | Di.SSPA |
| ARO7 | チポラ ロッサ ディ アクアヴィーヴァ | 40°53’13.47″ N 16°50’23.783” E | Di.SSPA |
| ARO8 | チポラ ロッサ ディ アクアヴィーヴァ | 40°53’18.816″ N 16°49’33.888” E | Di.SSPA |
| ARO9 | チポラ ロッサ ディ アクアヴィーヴァ | 40°54'51.372インチ N 16°49'3.504 E | Di.SSPA |
| ARO10 | チポラ ロッサ ディ アクアヴィーヴァ | 40°54’1.188″ N 16°49’24.311” E | Di.SSPA |
| ARO11 | チポラ ロッサ ディ アクアヴィーヴァ | 40°52'49.8インチ N 16°49'48.575 E | Di.SSPA |
| ARO12 | チポラ ロッサ ディ アクアヴィーヴァ | 40°52’38.892″ N 16°49’28.379” E | Di.SSPA |
| ARO13 | チポラ ロッサ ディ アクアヴィーヴァ | 40°53’21.768″ N 16°49’29.711” E | Di.SSPA |
| トロ1 | チポラ ロッサ ルンガ ディ トロペア | – | Di.SSPA |
| トロ2 | チポラ ロッサ トンダ ディ トロペア | – | Di.SSPA |
| MCO | チポラ ラマタ ディ モントロ | – | Di.SSPA |
| y Di.SSPA、土壌、植物、食品科学科、バーリ大学。 |
人口あたり 20 の遺伝子型の葉の材料をサンプリングし、使用するまで-80 ° C で保存しました。 多糖類が豊富な種の場合、 A.セパ、 多糖類を除去する最初のステップは、高品質の DNA を得るために不可欠です。 【52]. CTAB法に従って全DNAを抽出した 【53] そして最後に、Nano Drop 2000 UV-vis分光光度計(ThermoScientific、ウォルサム、マサチューセッツ州、米国)および0.8%アガロースゲル電気泳動により、品質と濃度をチェックしました。
SSR分析
によって開発された 16 の EST-SSR プライマーの組み合わせ 【54] および以前に遺伝的多様性研究でテストされました 【43] および 【44] および21のゲノムSSR [45~55】 それらの適合性を評価するためにスクリーニングされました(補足表S4)。 ジェノタイピングは、M13 テールが各フォワード SSR プライマーに追加される経済的な蛍光タグ付け法を使用して実行されました。 【56]. PCR ミックスは、20 ng の全 DNA、50 mM の dNTP ミックス、0.2X の PCR 反応バッファー、1 U の DreamTaq DNA ポリメラーゼ (Thermo Scientific、ウォルサム、マサチューセッツ州、米国)、0.8 gM のリバース プライマーを含む 0.16 μL の反応液で調製しました。 、M13配列(5'-TGTAAAACGACGGCCAGT-3')で伸長された0.032gMのフォワードプライマー、およびFAMまたはNED蛍光色素で標識された0.08gMのユニバーサルM13プライマー(Sigma-Aldrich、セントルイス、ミズーリ州、米国)。 PCR反応は、SimpliAmp(Applied Biosystems、CA、USA)サーモサイクラーで、大部分のプライマーペアに対して次の条件で実行されました:0.032°Cで13分間、5°Cで3秒間0.08サイクル、13°C 94 s および 5 °C で 40 s、最終伸長は 94 °C で 30 分間。 ACM58およびACM45に関しては、タッチダウンPCRを適用し、72°Cから45°Cで72サイクル、5°Cで446サイクル、その後449°Cで60分間の最終伸長を行いました。 PCR産物を55ウェルプレートにロードし、10 gLのHi-Diホルムアミド(Life Technologies、Carlsbad、CA、USA)および30 gL GeneScan 55 ROX Size Standard(Life Technologies、Carlsbad、CA、USA)と混合しました。 アンプリコンは、ABI PRISM 5 Avant Genetic Analyzer (Life Technologies、Carlsbad、CA、USA) キャピラリー シーケンス マシンによって解決されました。対立遺伝子は共優性としてスコア付けされ、GeneMapper ソフトウェア バージョン 72 を使用して割り当てられました。
ソフトウェア GenAlEx 6.5 【57] およびCervus 3.0.7 【58] 対立遺伝子の数 (Na)、有効な対立遺伝子の数 (Ne)、観察されたヘテロ接合性 (Ho)、予想されるヘテロ接合性 (He)、多型情報量 (PIC)、シャノンの情報指数 (I)、固定指数 (Fis) を推定するために使用されました。 ) 各 SSR 軌跡。
遺伝的多様性の評価
タマネギ集団間およびタマネギ集団内の遺伝的変異の階層的分割は、GenAlEx 6.5 によって評価されました。 【57] 有意性をテストするための 999 ブートストラップを使用した分子分散分析 (AMOVA) を通じて。 さらに、GenAlEx 6.5 ソフトウェアを使用して、すべての SSR 遺伝子座の Ho、He、および Fis の平均を計算することにより、各集団内の多様性を推定しました。
母集団構造は、STRUCTURE v.2.3.4 ソフトウェアに実装されているベイジアン モデル ベースのクラスタリング アルゴリズムによって推測されました。 【59]. データセットは、1 から 10 の範囲の多数の仮想クラスター (K) で実行され、各 K 値ごとに 100,000 回の独立した実行が設定されました。 実行ごとに、結果の一貫性を検証することを目的として、100,000 回の初期バーンイン期間と XNUMX 回のマルコフ連鎖モンテカルロ (MCMC) 反復が、混合モデルと集団間の独立した対立遺伝子頻度の下で実行されました。 最も可能性の高い K 値は、AK メソッドを実装して決定されました。 【60]、Web ベースのプログラム STRUCTURE HARVESTER で 【61]. メンバーシップ係数 (q 値) が 0.7 よりも高い場合、個々の集団は特定のクラスターに割り当てられました。それ以外の場合は、混合祖先と見なされました。
Neiの遺伝的距離行列によって明らかにされた系統間の遺伝的関係のパターンを視覚化するために、主座標分析が実行されました(補足表S5)。 対立遺伝子頻度に基づいて、POPTREEW ソフトウェアで算術平均 (UPGMA) クラスター分析を使用した重み付けされていないペア グループ法を実装して、遺伝的距離のデンドログラムを作成しました。 【62]. データセットのリサンプリングを 100 に設定して、階層的クラスタリングの信頼性を評価するためにブートストラップが適用されました。 最後にMEGA Xソフト 【63] 樹木描画ソフトとして使用しました。
補足資料: 以下はオンラインで利用可能です http://www.mdpi.com/2223-7747/9/2/260/s1. 表 S1: ARO、MCO、および TRO 球根の形態学的特徴付け。 表 S2: ARO 在来種と TRO および MCO 在来種について計算されたヘテロ接合性および固着指数。 表 S3: Fpt パラメータのペアワイズ値。 表 S4: 研究で使用された SSR のリスト。 表 S5。 Nei 遺伝的距離のペアワイズ母集団行列。 図 S1: Evanno のデルタ K で変化する K 値の折れ線グラフ。
投稿者の投稿: CL と LR は研究を考案し、実験を設計しました。 CL と PI は分子マーカー分析を行いました。 ARM と VZ が実地試験を実施しました。 RM、SP、GR、および CL がデータ分析に関与しました。 RM と CL が原稿を書きました。 すべての著者は、原稿の公開版を読み、同意しました。
資金調達: この作品は、地域のアプリア プロジェクト「アプリア野菜種の生物多様性」によって資金提供されました — Programma di Sviluppo Rurale per la Puglia 2014-2020. ミスラ 10—ソットミスラ 10.2; 助成金 CUP H92C15000270002、イタリア。
謝辞: 謝辞は、実験で使用される植物材料を提供するための「Azienda Agricola Iannone Anna」および「Associazione produttori della vera cipolla rossa di Acquaviva」によるものです。
利益相反: 著者らは、利害の対立を宣言していない。
参考文献
- 1. Stearn, WT 知られているアリウムの種は何種類ありますか? キューマグ。 1992, 9、180-182。 [CrossRef]
- 2.FAOSTAT。 FAO 統計データベース。 オンラインで入手可能: http://www.fao.org/2017 (8年2019月XNUMX日にアクセス)。
- 3. ブロック、E. ニンニクとタマネギの化学。 サイ。 午前 1985, 252、114-119。 [CrossRef]
- 4.リー、B。 ユング、JH; Kim, HS ラットの抗酸化活性に対するレッドタマネギの評価。 食品化学。 トキシコール。 2012, 50、3912-3919。 [CrossRef]
- 5.リー、SM。 ムーン、J。 チョン、JH。 チャ、YJ; Shin, MJ ラットの動脈血栓症に対するケルセチンが豊富なタマネギの皮抽出物の効果。 食品化学。 トキシコール。 2013, 57、99-105。 [CrossRef] [PubMed]
- 6. 吉成 理塩島 由美; Igarashi, K. zucker 糖尿病脂肪ラットにおけるタマネギ抽出物の抗肥満効果. 栄養素 2012, 4,1518-1526。 [CrossRef]
- 7.アカシュ、MSH。 レーマン、K. Chen, S. 香辛料植物 Allium cepa: 2 型糖尿病の治療のための栄養補助食品。 栄養 2014, 30、1128-1137。 [CrossRef] [PubMed]
- 8. Wang, Y.; ティアン、WX; タマネギのMa、XF抑制効果 (ネギ L.) 脂肪酸シンターゼの阻害による癌細胞および脂肪細胞の増殖に対する抽出物。 アジア太平洋。 J.がん 2012,13、5573-5579。 [CrossRef] [PubMed]
- 9.ライ、WW; スー、サウスカロライナ州; Chueh、FS; チェン、YY; ヤン、JS。 リン、JP; リエン、JC。 ツァイ、CH; Chung, JG ケルセチンは、NF-κB およびマトリックスメタロプロテイナーゼ-2/-9 シグナル伝達経路の阻害により、SAS ヒト口腔癌細胞の移動と浸潤を阻害します。 AnticancerRes。 2013, 33、1941-1950。 [PubMed]
- 10.ニカストロ、HL。 ロス、SA; Milner, JA ニンニクとタマネギ: がん予防特性. がん 解像度 2015, 8,181-189。 [CrossRef]
- 11.フォルテ、L。 トリチェリ、P。 ボアニニ、E。 ガザノ、M。 ルビーニ、K. フィニ、M。 Bigi、A.ケルセチン官能化ヒドロキシアパタイトの抗酸化および骨修復特性:in vitro骨芽細胞 - 破骨細胞 - 内皮細胞共培養研究。 ActaBiomater。 2016, 32、298-308。 [CrossRef]
- 12. ヤマザキ ヨウ。 岩崎 浩一三上 雅史; Yagihashi, A. XNUMX つのアリウム野菜における XNUMX のフレーバー前駆体、S-Alk(en)yl-L-システイン誘導体の分布。 食品科学技術。 解像度 2011, 17、55-62。 [CrossRef]
- 13. ブロック、E. アリウム属の有機硫黄化学 - 硫黄の有機化学への影響。 アンゲヴァンテ。 化学。 Int。 エド。 Engl。 1992, 31、1135-1178。 [CrossRef]
- 14. グリフィス、G.; トゥルーマン、L.; T.クラウザー; トーマス、B。 スミス、B. 玉ねぎ - 健康への世界的な利益。 フィトザー。 解像度 2002,16、603-615。 [CrossRef]
- 15. Schwimmer、S.; Weston, WJ 辛味の尺度としてのタマネギ中のピルビン酸の酵素的発達。 J.Agric。 食品化学。 1961, 9、301-304。 [CrossRef]
- 16.ケッター、CAT。 Randle, WM タマネギの辛味評価。 の 実験室教育のための試験済み研究; ケルヒャー、SJ、エド。 生物学研究所教育協会 (ABLE): ニューヨーク、ニューヨーク、米国、1998 年。 第 19 巻、177 ~ 196 ページ。
- 17. ハネルト、P 分類学、進化、および歴史。 の タマネギと関連作物、巻。 I. 植物学、生理学および遺伝学; Rabinowitch, HD, Brewster, JL, Eds.; CRC Press: ボカラトン、フロリダ州、米国、1990 年。 1-26ページ。
- 18.ラビノウィッチ、HD。 カーラ、L. アリウム作物科学:最近の進歩。 CABI パブリッシング: ウォリングフォード、英国、2002 年。
- 19.マラー、C。 カラベド、M。 エストパナン、G.; Mallor, F. タマネギの遺伝資源のキャラクタリゼーション (ネギ L.) 多様性のスペイン中等センターから。 スパン。 J.Agric. 解像度 2011, 9、144-155。 [CrossRef]
- 20. フェリオリ、F.; D'Antuono, LF イタリアとウクライナ産の地元のタマネギとエシャロット生殖質におけるフェノール類とシステイン スルホキシドの評価。 ジュネット。 リソース。 作物の進化。 2016, 63、601-614。 [CrossRef]
- 21.ペトロプロス、SA。 フェルナンデス、A。 バロス、L.; フェレイラ、ICFR。 Ntatsi, G. 'vatikiotiko' の形態学的、栄養学的および化学的記述、ギリシャからのタマネギの地元の在来種。 食品化学。 2015,182、156-163。 [CrossRef]
- 22. Liguori、L.; アディレッタ、G.; ナザロ、F.; Fratianni、F.; ディ・マッテオ、M。 Albanese、D.地中海地域のさまざまなタマネギ品種の生化学的、抗酸化特性、および抗菌活性。 J.Food Meas. キャラクター。 2019,13、1232-1241。 [CrossRef]
- 23.ユー、KS; パイク、L.; クロスビー、K. ジョーンズ、R。 Leskovar, D. 品種、生育環境、球根サイズによるタマネギの辛味の違い。 科学。 ホルティック。 2006,110、144-149。 [CrossRef]
- 24.ビースク、N.; パーナー、H。 シュワルツ、D.; ジョージ、E。 Kroh、LW。 Rohn, S. 遺伝子型の影響を受けるタマネギ球根 (Allium cepa L.) のさまざまな部分におけるケルセチン-3、4'-O-ジグルコシド、ケルセチン-4'-O-モノグルコシド、およびケルセチンの分布。 食品化学。 2010,122、566-571。 [CrossRef]
- 25. カルーソ、G.; コンティ、S。 ヴィラリ、G. ボレッリ、C。 Melchionna、G.; ミヌトロ、M。 ルッソ、G. Amalfitano, C. タマネギの収量、品質、抗酸化物質含有量に対する移植時期と植物密度の影響 (ネギ L.) 南イタリアで。 科学。 ホルティック。 2014,166、111-120。 [CrossRef]
- 26.ペレス・グレゴリオ、MR。 レゲイロ、J. シマルガンダーラ、J.; ロドリゲス、AS; アルメイダ、DPF 抗酸化フラボノイドの供給源としてタマネギの付加価値を高める: 重要なレビュー。 クリティカル 食品科学大臣 Nutr。 2014, 54、1050-1062。 [CrossRef] [PubMed]
- 27. Pohnl、T.; シュヴァイガート、RM; Carle, R.タマネギの可溶性炭水化物と辛味成分に対する栽培方法と品種選択の影響 (ネギ L.)。 J.Agric。 食品化学。 2018, 66、12827-12835。 [CrossRef] [PubMed]
- 28.テデスコ、I。 カーボン、V。 Spagnuolo、C。 ミナシ、P。 Russo, GL 南イタリアの XNUMX 品種のフラボノイドの同定と定量 アリウムセパ L.、Tropea (赤タマネギ)、Montoro (銅タマネギ)、および酸化ストレスからヒト赤血球を保護する能力。 J.Agric。 食品化学。 2015, 63、5229-5238。 [CrossRef]
- 29. Villano, C.; Esposito、S。 カルッチ、F.; フルシアンテ、L.; カルプト、D.; Aversano, R. タマネギのハイスループット ジェノタイピングにより、遺伝的多様性の構造と分子育種に役立つ有益な SNP が明らかになります。 モル。 繁殖。 2019, 39、5。 [CrossRef]
- 30.メルカティ、F。 ロンゴ、C。 ポマ、D。 アラニティ、F。 ルピニ、A。 マンマノ、MM; フィオーレ、MC; Abenavoli、MR; Sunseri, F イタリアの長期保存用トマトの遺伝子変異 (ソラナム・リコペルシカム L.) SSR と形態学的果実形質を使用したコレクション。 ジュネット。 リソース。 作物の進化。 2014, 62、721-732。 [CrossRef]
- 31.ゴンザレス・ペレス、S。 マラー、C。 Garces-Claver、A。 メリノ、F。 タボアダ、A。 リベラ、A。 ポマール、F。 ペロビッチ、D.; Silvar, C. タマネギのコレクションにおける遺伝的多様性と品質特性の調査 (ネギ L.) スペイン北西部の在来種。 遺伝学 2015, 47、885-900。 [CrossRef]
- 32. Lotti、C.; Iovieno、P。 セントマニ、I.; アーカンソー州マルコトリジャーノ。 ファネリ、V。 ミミオラ、G.; Summo, C.; パヴァン、S。 Ricciardi, L. ケールの遺伝的、生物農業的、および栄養学的特徴付け (アブラナ属 L. var。 アセファラ) 南イタリア、プーリア州の多様性。 多様性 2018,10、25。 [CrossRef]
- 33.バルダロ、N.; アーカンソー州マルコトリジャーノ。 ブラクト、V。 マゼオ、R.; Ricciardi、F。 ロッティ、C。 パヴァン、S。 Ricciardi, L. 耐性の遺伝子解析 オロバンチェ クレナータ (Forsk.) エンドウ豆 (エンドウ L.) 低ストリゴラクトンライン。 J. Plant Pathol。 2016, 98、 671-675。
- 34. 和光徹塚崎 浩; 矢口 誠; 山下一浩; 伊藤 誠; 執行正則. タマネギ房の抽だい時期に関する量的形質遺伝子座のマッピング (ネギフィスツロスム L.)。 ユーフィティカ 2016, 209、537-546。 [CrossRef]
- 35.ダッカ、ノースカロライナ。 Mukhopadhyay、A。 パリトッシュ、K. グプタ、V。 Pental、D.; Pradhan, AK 遺伝子 SSR の同定と SSR ベースの連鎖地図の構築 ブラシカジュンセア。 ユーフィティカ 2017, 213、15。 [CrossRef]
- 36.アナンダン、S。 モテ、SR; Gopal, J. SSR マーカーを使用したタマネギ品種の同一性の評価。 種子科学技術。 2014, 42、279-285。 [CrossRef]
- 37. Mitrova、K.; Svoboda、P。 Ovesna, J. チェコ共和国産のタマネギ品種を区別するためのマーカー セットの選択と検証。 チェコの J. ジュネ。 植物の品種。 2015, 51、62-67。 [CrossRef]
- 38.ディ・リエンツォ、V。 Miazzi、MM; ファネリ、V。 サベッタ、W。 Montemurro、C.プーリアのオリーブ遺伝資源の生物多様性の保存と特徴付け。 アクタ・ホルティック。 2018,1199、1-6。 [CrossRef]
- 39.マラー、C。 Arnedo-Andres、A.; Garces-Claver, A. スペイン語の遺伝的多様性の評価 アリウムセパ マイクロサテライトマーカーを使用したタマネギ育種のための在来種。 科学。 ホルティック。 2014,170、24-31。 [CrossRef]
- 40. リベラ、A.; マラー、C。 Garces-Claver、A。 Garcia-Ulloa、A.; ポマール、F。 Silvar, C. タマネギの遺伝的多様性の評価 (アリウムセパ L.) スペイン北西部の在来種とヨーロッパの変動性との比較。 NZJ クロップホーティック。 2016, 44、103-120。 [CrossRef]
- 41. De Giovanni, C.; パヴァン、S。 タラント、F。 ディ・リエンツォ、V.; Miazzi、MM; アーカンソー州マルコトリジャーノ。 マンジーニ、G. モンテムロ、C. リカルディ、L.; Lotti, C. ひよこ豆の世界的な生殖質コレクションの遺伝的変異 (Cicer arietinum) L.) 遺伝的浸食のリスクがあるイタリアの登録を含む。 生理。 モル。 生物。 植物 2017, 23、197-205。 [CrossRef]
- 42.マゼオ、R。 モルゲス、A.; ソナンテ、G. ズルアガ、DL; パヴァン、S。 リカルディ、L.; Lotti, C. ブロッコリーラーベの遺伝的多様性 (アブラナ L.亜種。 シルベストリス (L.) Janch.) 南イタリア出身。 科学。 ホルティック。 2019, 253、140-146。 [CrossRef]
- 43. Jakse、M.; マーティン、W。 マッカラム、J.; Havey, M. タマネギ品種識別のための一塩基多型、インデル、および単純な配列反復。 混雑する。 社会ホルティック。 科学。 2005,130、912-917。 [CrossRef]
- 44.マッカラム、J。 トムソン、S。 Pither-Joyce、M。 Kenel, F. 表現された配列タグ単純配列反復マーカーに基づく栽培球根タマネギにおける遺伝的多様性分析および一塩基多型マーカーの開発。 混雑する。 社会ホルティック。 科学。 2008,133、810-818。 [CrossRef]
- 45.ボールドウィン、S。 Pither-Joyce、M。 ライト、K.; チェン、L.; McCallum, J. タマネギ内およびタマネギ間の遺伝的多様性を推定するための堅牢なゲノム単純配列反復マーカーの開発 (ネギ L.) 集団。 モル。 繁殖。 2012, 30、1401-1411。 [CrossRef]
- 46. ジャワ州デウッディ。 ハニーカット、RL; Skow、LC オジロジカのマイクロ サテライト マーカー。 J. ヘレド。 1995, 86、 317-319。 [CrossRef] [PubMed]
- 47. Khodadadi、M.; Hassanpanah、D. イランのタマネギ (ネギ L.) 近親交配の抑制に対する品種の反応。 世界のアプリケーション。 科学。 J. 2010,11、426-428。
- 48.アブドゥ、R。 バカソ、Y. 佐渡, M.; 日本、ボードイン; Hardy, OJ ニジェールタマネギの遺伝的多様性 (ネギ L.) シンプル シーケンス リピート マーカー (SSR) によって評価されます。 アクタ・ホルティック。 2016,1143、 77-90。 [CrossRef]
- 49.パヴァン、S。 ロッティ、C。 アーカンソー州マルコトリジャーノ。 マゼオ、R.; バルダロ、N.; ブラクト、V。 Ricciardi、F。 タラント、F。 D'Agostino、N.; Schiavulli、A。 ら。 ゲノムワイドなマーカーの発見とジェノタイピングによって明らかにされた、栽培されたひよこ豆の明確な遺伝子クラスター。 植物ゲノム 2017, 2017、10. [CrossRef]
- 50.パヴァン、S。 アーカンソー州マルコトリジャーノ。 Ciani、E。 マゼオ、R.; ゾンノ、V。 Ruggieri、V。 ロッティ、C。 Ricciardi, L. メロンのジェノタイピングによる配列決定 (ククミスメロ L.) 二次的な多様性の中心地からの生殖質コレクションは、異なる遺伝子プールの遺伝的変異とゲノムの特徴のパターンを浮き彫りにします。 BMCジェノム。 2017, 18、59。 [CrossRef]
- 51.ディ・リエンツォ、V。 シオン、S。 タラント、F。 D'Agostino、N.; モンテムロ、C. ファネリ、V。 サベッタ、W。 Boucheffa、S。 タメンジャリ、A。 Pasqualone、A。 ら。 地中海盆地内のオリーブ個体群間の遺伝的流れ。 ピア J. 2018, 6. [CrossRef]
- 52.シェパード、LD。 McLay, TG 多糖類が豊富な植物組織から DNA を分離するための XNUMX つのマイクロスケール プロトコル。 J.Plant Res. 2011,124、311-314。 [CrossRef]
- 53.ドイル、JJ。 Doyle, JL 新鮮な組織からの植物 DNA の分離。 フォーカス 1990,12、13-14。
- 54.クール、JC。 チャン、F。 喬平、Y.; マーティン、W。 Zewdie、Y.; マッカラム、J.; カタナック、A. ラザフォード、P。 シンク、KC; ジェンデレク、M。 ら。 11,008 個のタマネギ発現配列タグのユニークなセットにより、単子葉目アスパラガル目と子馬目の間の発現配列とゲノムの違いが明らかになります。 植物細胞 2004,16、114-125。 [CrossRef]
- 55.キム、HJ。 リー、HR; ヒョン、JY; 歌、KH; キム、KH; キム、JE。 ハー、CG; Harn, CH SSR Finder を使用したタマネギの遺伝的純度検査のためのマーカーの開発。 韓国のJ.ブリード。 科学。 2012, 44、421-432。 [CrossRef]
- 56. Schuelke, M. PCR フラグメントの蛍光標識のための経済的な方法。 Nat。 バイオテクノロジー。 2000, 18、233-234。 [CrossRef] [PubMed]
- 57. Peakall、R.; Smouse、PE GenAlEx 6.5: Excel での遺伝子解析。 教育と研究のための集団遺伝ソフトウェア: 更新。 バイオインフォマティクス 2012, 28、2537-2539。 [CrossRef] [PubMed]
- 58.カリノフスキー、ST。 テーパー、ML; Marshall, TC コンピュータ プログラム CERVUS が遺伝子型決定エラーに対応する方法を修正すると、父子鑑定の成功率が向上します。 モル。 Ecol。 2007,16、1099-1106。 [CrossRef]
- 59.プリチャード、JK。 スティーブンス、M.; ローゼンバーグ、NA; Donnelly、P. 構造化された母集団における関連マッピング。 午前。 J.ハム。 ジュネット。 2000, 67、 170-181。 [CrossRef]
- 60. エヴァンノ、G.; Regnaut、S。 Goudet, J. ソフトウェア STRUCTURE を使用した個人のクラスター数の検出: シミュレーション研究。 モル。 Ecol。 2005,14、2611-2620。 [CrossRef]
- 61.アール、D。 VonHoldt, B. STRUCTURE HARVESTER: STRUCTURE 出力を視覚化し、Evanno メソッドを実装するための Web サイトとプログラム。 保存します。 ジュネット。 リソース。 2011, 4. [CrossRef]
- 62. 竹崎直子; ネイ、M.; Tamura, K. POPTREEW: 対立遺伝子頻度データから集団ツリーを構築し、その他の量を計算するための POPTREE の Web バージョン。 モル。 Biol。 Evol。 2014, 31、 1622-1624。 [CrossRef]
- 63.クマール、S。 Stecher、G.; リー、M。 Knyaz、C。 Tamura、K. MEGA X. コンピューティング プラットフォーム全体の分子進化遺伝学分析。 モル。 Biol。 Evol。 2018, 35、1547-1549。 [CrossRef]